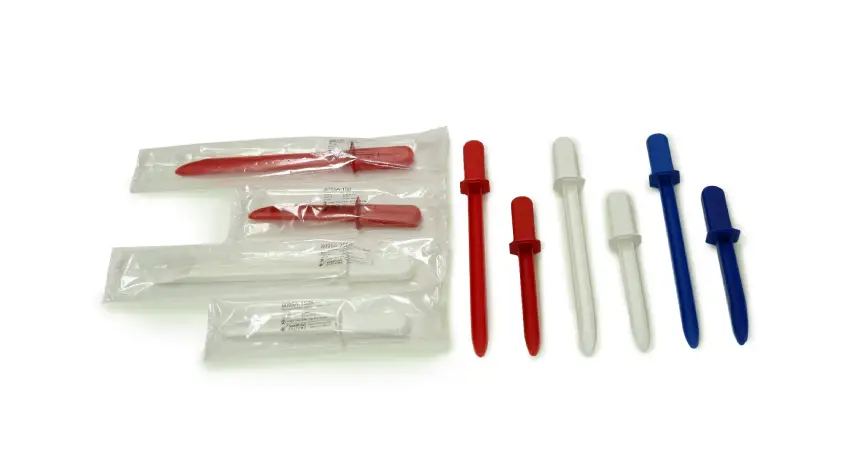
Laboratórios acreditados operam sob rigorosos padrões de qualidade e rastreabilidade, principalmente quando seguem as diretrizes da norma ISO/IEC 17025, que rege os requisitos gerais para competência de laboratórios de ensaio e calibração. Nesses ambientes, o uso de insumos e instrumentos deve ser meticulosamente documentado, e isso inclui o Amostrador Estéril.
Utilizado para coletar amostras microbiologicamente seguras de líquidos, sólidos ou pós, o Amostrador Estéril só pode ser integrado a rotinas laboratoriais acreditadas quando acompanhado de uma documentação robusta, rastreável e compatível com os critérios normativos exigidos.
Neste artigo, você vai conhecer as principais documentações exigidas para o uso de Amostrador Estéril em laboratórios acreditados, como elas devem ser organizadas e de que forma impactam o cumprimento de auditorias internas e externas.
O papel do Amostrador Estéril em laboratórios com acreditação
O Amostrador Estéril é fundamental para garantir a integridade e representatividade das amostras, principalmente na área microbiológica, farmacêutica, ambiental e de controle de qualidade de alimentos. Em um laboratório acreditado, qualquer falha na rastreabilidade ou no controle de esterilidade pode invalidar os resultados obtidos — por isso, a documentação associada a esse equipamento precisa ser completa e precisa.
Não basta que o amostrador esteja esterilizado: é necessário comprovar, registrar e manter histórico de cada lote, de cada uso e de sua validade técnica.
1. Ficha técnica do produto
O primeiro documento obrigatório para o uso de um Amostrador Estéril é a ficha técnica fornecida pelo fabricante. Este documento descreve:
- Material de composição (ex: polipropileno virgem, PEAD)
- Dimensões, capacidade e peso
- Método de esterilização aplicado (radiação gama, óxido de etileno, etc.)
- Recomendação de uso (para líquidos, sólidos, pós)
- Compatibilidade com áreas classificadas e salas limpas
- Condições de armazenamento e transporte
- Temperatura máxima suportada (quando autoclavável)
A ficha técnica deve estar disponível para consulta no laboratório e anexada aos registros de validação de processos, quando aplicável.
2. Certificado de esterilidade
Todo Amostrador Estéril deve ser acompanhado por um certificado de esterilidade emitido por laboratório terceirizado ou pelo próprio fabricante, desde que este possua acreditação para o serviço.
Esse certificado deve conter:
- Número do lote do amostrador
- Data de esterilização
- Método utilizado e condições do processo (dose de radiação, concentração de ETO, tempo de exposição)
- Resultado da validação microbiológica (ex: esterilidade garantida até 10â»â¶)
- Assinatura técnica e CNPJ do laboratório emissor
A Soluções Axios Brasil, por exemplo, entrega Amostradores Estéreis com laudos de esterilização por lote, garantindo confiabilidade ao usuário final.
3. Certificado de conformidade do lote
Esse documento atesta que o lote de Amostrador Estéril fabricado atende aos critérios de qualidade estabelecidos pelo fabricante e, sempre que possível, pelos órgãos reguladores.
O certificado de conformidade deve apresentar:
- Nome comercial e referência do produto
- Número do lote e data de fabricação
- Laudos de inspeção do lote (visuais, dimensionais e microbiológicos)
- Nome da empresa responsável e CNPJ
- Garantia de que o lote foi aprovado para uso
Esse documento é frequentemente solicitado em auditorias e pode ser exigido por clientes que recebem laudos emitidos pelo laboratório.
4. Registro de recebimento e controle de estoque
Ao receber um lote de Amostrador Estéril, o laboratório deve registrá-lo em seu sistema interno. Isso inclui:
- Data de entrada
- Quantidade recebida
- Lote e validade dos produtos
- Condições da embalagem no recebimento
- Responsável pelo recebimento e inspeção visual
Esses registros são importantes para garantir que nenhum produto vencido, danificado ou fora da especificação entre na área técnica do laboratório.
5. POP de utilização e descarte
Todo laboratório acreditado deve possuir um Procedimento Operacional Padrão (POP) específico para o uso e descarte de Amostrador Estéril. Esse documento define as etapas operacionais e os cuidados necessários para garantir a qualidade da coleta.
O POP deve conter:
- Local adequado de abertura da embalagem
- Métodos de higienização do ambiente e dos EPIs
- Orientações sobre tempo máximo entre abertura e uso
- Instruções para descarte após a coleta
- Referência aos documentos de rastreabilidade do amostrador
Esse procedimento é analisado durante auditorias da ISO/IEC 17025 e deve estar sempre atualizado.
6. Registro de uso vinculado à amostra
Em laboratórios acreditados, cada uso do Amostrador Estéril deve estar vinculado a uma amostra específica. Isso significa que é necessário registrar:
- Código da amostra
- Lote do amostrador utilizado
- Responsável técnico pela coleta
- Data e horário da amostragem
- Tipo de material coletado (líquido, sólido, pó)
Esse nível de rastreabilidade é indispensável para assegurar a confiabilidade do resultado e para atender exigências em casos de investigação de desvios ou análises repetidas.
7. Laudos de compatibilidade com produtos sensíveis
Em algumas análises, especialmente na indústria farmacêutica e cosmética, é necessário comprovar que o Amostrador Estéril não libera substâncias interferentes na amostra. Nesses casos, o fornecedor deve apresentar:
- Laudo de ausência de endotoxinas
- Testes de ausência de metais pesados
- Validação de compatibilidade com pH extremos ou solventes
- Declaração de atoxidade do material
Esses documentos aumentam a segurança do processo e permitem o uso do amostrador em análises que exigem grau farmacêutico.
8. Documentação ambiental (quando aplicável)
O descarte de Amostradores Estéreis usados deve seguir a Política Nacional de Resíduos Sólidos. Assim, o laboratório deve manter registros de:
- Quantidade descartada por mês
- Classificação do resíduo (grupo A ou grupo B)
- Nome e licença da empresa coletora
- Formulário de Manifesto de Transporte de Resíduos (MTR)
Essas informações fazem parte do conjunto documental exigido em auditorias ambientais ou pela vigilância sanitária.
A importância do fornecedor nesse processo
A qualidade da documentação associada ao Amostrador Estéril começa com o fornecedor. A Soluções Axios Brasil é referência no mercado por fornecer amostradores com:
- Ficha técnica completa
- Laudos de esterilização validados
- Certificados de conformidade por lote
- Etiquetas com rastreabilidade total
- Suporte técnico para integração em sistemas de qualidade
Ao optar por fornecedores que já operam com foco em laboratórios acreditados, o processo de adequação documental se torna mais ágil, seguro e confiável.
Documentação é parte do controle da qualidade
O uso do Amostrador Estéril em laboratórios acreditados exige muito mais do que conhecimento técnico: exige documentação precisa, padronizada e rastreável. A ficha técnica, os laudos de esterilização, os certificados de conformidade, os POPs internos e os registros de uso são os pilares que sustentam a confiabilidade dos resultados gerados.
Ignorar qualquer uma dessas exigências pode comprometer auditorias, gerar não conformidades e até invalidar análises críticas. Por isso, contar com fornecedores como a Soluções Axios Brasil, que entregam produtos com documentação completa e pronta para auditoria, é o caminho mais seguro para garantir qualidade, confiança e credibilidade aos seus processos laboratoriais.